海洋所破解免疫抑制剂霉酚酸生物合成机制
近日,中国科学院海洋研究所海洋生物制造团队在真菌源免疫抑制剂霉酚酸(Mycophenolic acid, MPA)的生物合成机制研究中取得重大突破,破解了百年天然产物生物合成之谜,为高效生物制造提供新策略。该研究首次系统解析了MPA生物合成中类β-氧化途径的多酶级联过程,揭开了这一具有百余年历史的天然产物在合成途径上的最后谜团,为通过代谢工程提升药物产量提供了全新理论和技术支撑。相关成果已发表于Advanced Science。
霉酚酸于1893年被首次分离并结晶,是历史上第一个被发现的抗生素,具有里程碑式的天然产物地位。作为免疫抑制剂药物吗替麦考酚酯和麦考酚钠的活性成分,MPA被广泛用于器官移植和自身免疫性疾病的临床治疗。尽管其历史意义重大,但一个多世纪以来,MPA的生物合成遗传机制与酶催化基础一直未被完全阐明。
经过12年的系统研究,团队从一株短密青霉NRRL864(Pb864)中成功捕获了MPA生物合成基因簇(ChemBioChem. 2015),并综合运用基因敲除、异源表达、前体饲喂、体外酶活验证与亚细胞定位等多项技术,在国际上首次完整解析出MPA的生物合成途径,揭示其独特的“合成-降解耦合”机制及多细胞区室协同参与过程(PNAS. 2019),并先后解析了关键酶MpaH'(酰基辅酶A水解酶)和MpaG'(O-甲基转移酶)的晶体结构(FEBSJ. 2021; Protein Sci. 2024)。
本研究首次系统阐释了位于过氧化物酶体内的类β-氧化酶催化级联反应,该反应通过连续的氧化、脱水、还原、异构和逆克莱森缩合等步骤,完成两次侧链缩短循环,最终生成霉酚酸(图1)。研究新鉴定出多个酰基辅酶A连接酶,其中PbACL75显示更高的催化效率与底物宽泛性,显著优化了合成途径中的代谢流强度。进一步通过启动子工程对关键基因(包括过氧化物酶体限速酶PbACOX323、过氧化物酶体生因子PbPex337及内质网定位氧化酶MpaB')进行整合过表达,成功将霉酚酸产量从0.77 g/L提升至1.15 g/L,增幅近50%,充分展示了β-氧化途径工程在天然产物产量提升中的巨大潜力。
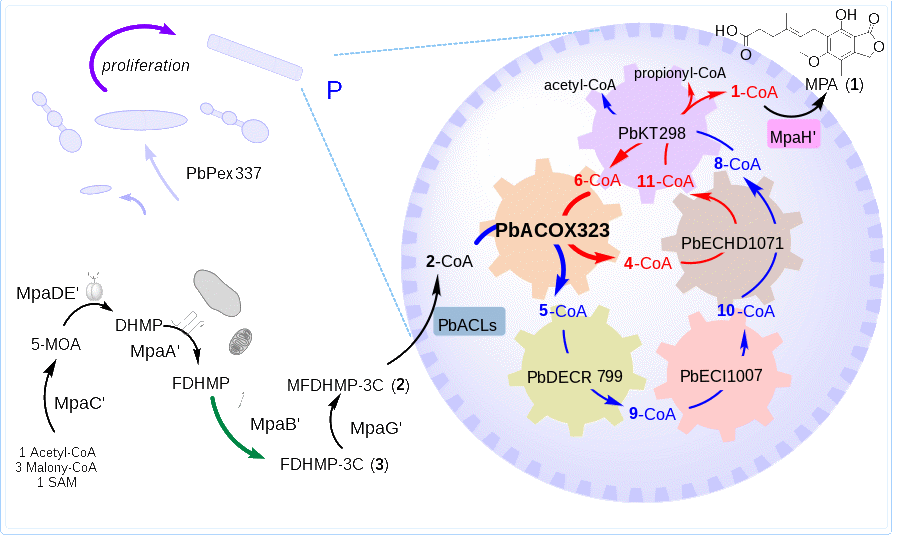
霉酚酸的完整区室化生物合成(图源自Advanced Science)
该研究不仅揭示自然界将经典的降解代谢β-氧化途径重编程以用于高值次级代谢产物合成的进化创新机制,也为通过区室化工程优化天然产物的生物合成系统提供了理论依据与工程蓝图。
中国科学院海洋研究所张伟研究员和山东大学微生物技术研究院李盛英教授为论文共同通讯作者,博士生范保强为第一作者。研究获得了国家自然科学基金、国家重点研发计划、山东省自然科学基金和深圳市基础研究计划等项目的支持。
论文信息:
B. Fan, Y. Liu, L. Chi, C. Yang, S. Li*, and W. Zhang*, Enhancing the β-Oxidation-Like Pathway for the Optimal Production of the Immunosuppressant Mycophenolic Acid.Adv. Sci. (2025): e08826.
附件下载:
 鲁公网安备37020202001323号
鲁公网安备37020202001323号 | 古镇口园区地址:青岛市西海岸新区海军路88号 南海路园区地址:青岛市市南区南海路7号 科考船码头基地:青岛市西海岸新区长江东路8号 |
邮编:266000 邮件:iocas@qdio.ac.cn 电话:0532-82898611 传真:0532-82898612 |
