海洋所成功构建两种靶向型海洋多糖抗肿瘤纳米载体
近日,中国科学院海洋研究所海藻化学与海洋药物课题组在开发海洋活性多糖抗肿瘤药物递送载体、实现肿瘤免疫微环境靶向调控研究方面取得重要进展。相关研究成果分别发表在国际期刊Carbohydrate Polymers与Materials Today Advances上。研究团队成功构建了两种靶向型海洋多糖纳米载体,实现化疗、免疫治疗与基因/抗血管生成治疗的多维协同,在动物模型中呈现出良好的肿瘤抑制作用,为胰腺癌、结直肠癌临床系统化治疗提供了新思路。
褐藻多糖硫酸酯具有天然P‑选择素靶向性与免疫调节活性,是构建肿瘤靶向递送载体的理想天然高分子材料。围绕“主动靶向+免疫协同”核心设计理念,针对不同实体瘤的临床治疗瓶颈,研究团队设计并构建了差异化的多功能纳米递送系统,有效克服了传统治疗中存在的靶向性差、药物联用效率低、免疫抑制微环境难逆转等难题。
在胰腺癌治疗方面,团队研发了一种磁靶向褐藻多糖纳米载体(Fuc@miR MNPs)。该载体以Fe₃O₄为磁核,负载5‑氟尿嘧啶修饰miR‑15a。外加磁场导航与P‑选择素亲和的双重富集作用,该系统有效突破荷瘤小鼠胰腺肿瘤致密的纤维化屏障,同步实现化疗杀伤、致癌基因沉默、免疫微环境逆转。体内实验表明,该系统在荷瘤小鼠模型中的抑瘤率高达75%(图1)。
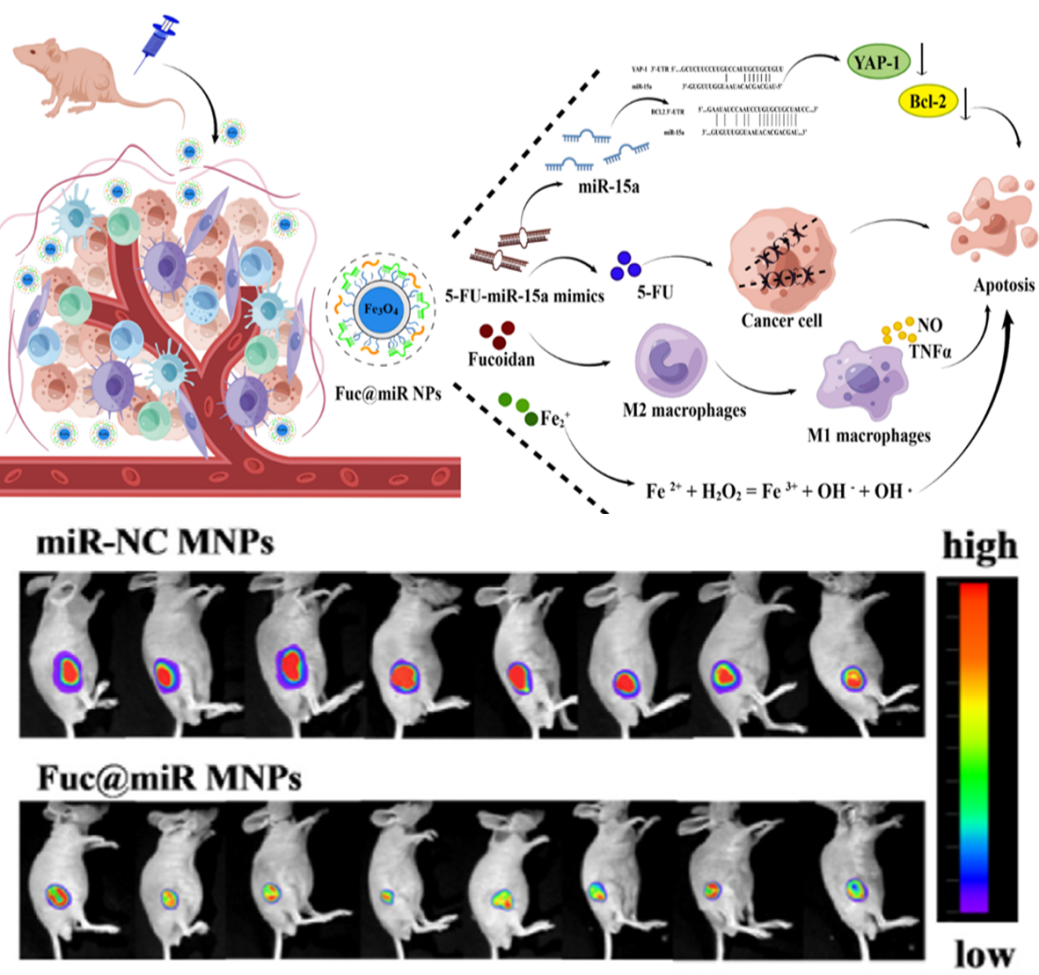
图1 多功能磁靶向纳米递送系统Fuc@miR MNPs在胰腺癌荷瘤小鼠中的应用
在结直肠癌治疗方面,团队构建了双靶向纳米载体(CS‑Arg/Fuc‑Bio@OF),用于同步递送奥沙利铂与呋喹替尼。该载体通过P‑选择素亲和与生物素受体双重主动靶向机制,实现了药物在荷瘤小鼠肿瘤部位的精准富集与酸性微环境响应释药。该系统协同实现免疫原性细胞死亡、肿瘤相关巨噬细胞M1极化、抗血管生成三重作用,从而高效抑制肿瘤增殖转移,且展现出优异的生物安全性(图2)。
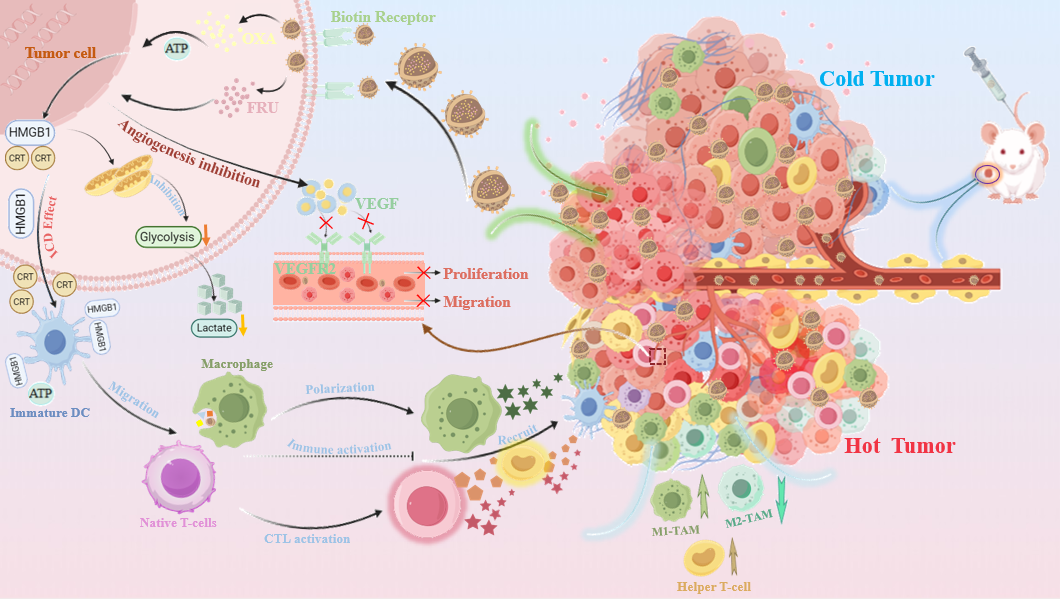
图2 双靶向纳米递送系统CS-Arg/Fuc-Bio@OF的构建及在结肠癌治疗中的应用
上述两项研究突破了传统纳米载体功能局限,成功将海洋多糖打造为集“靶向递送、药物控释、免疫激活”于一体多功能载体,为海洋生物资源高值化利用与抗肿瘤创新药物研发提供重要实验支持。
吴宁研究员、张全斌研究员为论文通讯作者,邓真真博士后、万家齐副研究员以及王慧博士研究生分别为论文第一作者。研究得到国家自然科学基金、中国科学院海洋所自主部署项目、中国博士后科学基金的共同资助。
论文信息:
1) Zhenzhen Deng#, Jiaqi Wan#, Suoqi Shan, Jing Wang, Lihua Geng, Yang Yue, Quanbin Zhang*, Ning Wu*. Delivery of 5-fluorouracil modified MicroRNAs by fucoidan-based magnetic nanoparticles to enhances tumor-localized immunotherapy and chemotherapy. Materials Today Advances, 2026. https://doi.org/10.1016/j.mtadv.2025.100646
2)Hui Wang, Haoyu Yu, Yan Yang, Mengying Fu, Lihua Geng, Jing Wang, Yang Yue, Quanbin Zhang, Ning Wu*. Synergistic induction of immunogenic cell death and tumor microenvironment remodeling by biotinylated marine polysaccharide nanoparticles for enhanced colorectal cancer therapy. Carbohydrate Polymers, 2026. https://doi.org/10.1016/j.carbpol.2026.125185
附件下载:
 鲁公网安备37020202001323号
鲁公网安备37020202001323号 | 古镇口园区地址:青岛市西海岸新区海军路88号 南海路园区地址:青岛市市南区南海路7号 科考船码头基地:青岛市西海岸新区长江东路8号 |
邮编:266000 邮件:iocas@qdio.ac.cn 电话:0532-82898611 传真:0532-82898612 |
